

6月11日-15日,2023第15届国际代谢工程大会(15th Metabolic Engineering Conference,简称ME15)在新加坡隆重举办。该大会由代谢工程领域的国际权威学术组织国际代谢工程学会(International Metabolic Engineering Society,简称IMES)主办。
本届大会围绕“代谢工程中的大数据与人工智能”“代谢工程与下一代医药”“合成生物学与代谢工程”“生物铸造厂:代谢工程中的自动化”“代谢工程与生物制造:从实验室到工业化”“代谢工程与下一代底盘”等议题展开,多方位展示了代谢工程领域近两年的最新科技成果及未来研究热点。
大会汇集了全球代谢工程领域的顶尖科学家,美国工程院外籍院士、韩国国家科学与工程院院士,现任韩国科学技术院长Sang Yup Lee,国际合成生物学产业化先驱、美国国家工程院院士、劳伦斯伯克利国家实验室、美国加州大学伯克利分校合成生物学工程研究中心主任Jay Keasling,荷兰代尔夫特理工大学工业微生物学教授兼生物技术系主任、荷兰科学界最高奖项史蒂文奖获得者Jack Pronk等,还有来自美国、德国、英国、中国、日本、韩国、新加坡等28多个国家的671位代谢工程领域专家学者及相关产业届代表参会,规模为历届之最。

大会现场图
6月14日会议期间,举行了重要的2023年度国际代谢工程奖(IMES Award)颁奖仪式,清华大学生命科学学院、化工系教授、合成与系统生物学中心主任陈国强为本届该奖项唯一获奖者,也是首个获得该项荣誉的中国大陆地区学者。同时,陈国强教授在ME15大会上作题为“Next Generation Industrial Biotechnology Based on Synthetic Biology of Halomonas spp.”的特邀报告,分享其在代谢工程领域的最新研究成果。

陈国强教授获国际代谢工程奖(IMES Award)
陈国强教授为全球顶尖合成生物学专家,代谢工程领域的领军型人物,清华大学教授、合成与系统生物学中心主任,国家973“合成生物学”项目以及国家重大专项项目的首席科学家,也是中国大陆首位国际代谢工程奖获得者。
陈国强教授同时在全球合成生物学顶级期刊 Synthetic and Systems Biotechnology(《合成和系统生物技术》,简称SSB)担任共同主编,并在国际学术期刊如Chemical Reviews 、Chemical Society Reviews等上共发表微生物技术和生物材料相关论文400多篇,Web of Science引用两万五千多次,H指数78。获得授权专利50多项,以及50个公开专利。
此次陈国强教授获得的国际代谢工程奖,由国际代谢工程学会发起,每两年授予一位在代谢工程领域做出卓越贡献的研究人员,并在其和美国化学工程师协会(AIChE)共同举办的国际代谢工程大会上颁奖。自2000年该奖项正式颁发以来,获奖者均来自海外,包括生物化学工程先驱James E.Bailey、合成生物学领域权威Jay Keasling,以及多位美国工程院院士等顶尖科学家,陈国强教授是首位获得该奖项的中国学者。
在颁奖典礼上,国际代谢工程奖评选委员会主席、韩国科学院化学与生物分子工程系杰出教授、代谢与生物分子工程国家实验室主任Sang Yup Lee院士介绍了该奖项的评审情况,他表示:“陈国强教授团队最初采用了基于传统微生物底盘的工业生物技术(CIB),如使用大肠杆菌等作为底盘,然而在放大过程中存在染菌的问题。这促使他对嗜盐菌Halomonas进行开发,避免了染菌问题,并且实现连续开放、无需灭菌的发酵过程,这一技术已被广泛采用并应用于化学品的开放生产。因此组委会决定将2023国际代谢工程奖颁发给陈国强教授,以表彰他通过开发嗜盐菌和‘下一代工业生物技术’对代谢工程领域做出的杰出贡献。恭喜陈国强教授!”

Sang Yup Lee院士(左)与陈国强教授(右)
资料显示,相较于传统化工制造,以合成生物学为核心的生物制造通常以可再生生物资源为原料,可摆脱对石油资源的依赖,降低能耗,大幅减少污染物生成,具有高效、绿色、可持续的优势特性。但由于微生物原有的生物系统限制,工业化生产过程中往往会遇到许多技术瓶颈。陈国强教授长期从事“生物合成PHA材料及其下一代工业生物技术(Next Generation Industrial Biotechnology, 简称NGIB)”的研究,利用合成生物学和代谢工程学方法,构建了更加符合规模化生产的工程菌株和技术体系,实现了生物制造产业关键核心技术的不断突破。
2005年,陈国强教授团队在位于世界最酷热、最干燥的地区之一、盐浓度达200克/升的中国新疆艾丁湖筛选出适应力最强的工业微生物菌株——嗜盐菌Halomonas,通过基因编辑、代谢网络调控等技术,重新构建了嗜盐菌的代谢网络,改造出适应能力更强、生长速度更快的菌株,并开发出适用于该底盘菌株的NGIB体系,覆盖了理论、模型、分子操作、实验室培养技术、中试技术及工业生产技术,以及部分产品的应用等。目前在该技术体系下,菌株已连续超过20代迭代。
相比于利用传统微生物底盘的工业生物技术(CIB),如大肠杆菌等,基于嗜盐菌的NGIB无需灭菌,生产过程可以开放和连续化,降低了能源和淡水消耗,并且降低了生物制造的复杂性和设备的制造成本,使生物制造产品竞争性得到增强。陈国强教授团队预测,NGIB能够将传统生物制造的能耗降低50%以上,并大幅提高生产效率。
对于获得2023年度国际代谢工程奖,陈国强教授表示:“我很荣幸能够得到这一奖项认可,也很激动能够再次与大家相聚在代谢工程领域的学术盛会。非常感谢国际学术界同仁一直以来的交流与帮助,是他们的杰出成就推动了代谢工程领域的发展,也非常感谢我的团队、学生为‘下一代工业生物技术’所作出的贡献。在各位学术同仁的努力下,代谢工程和合成生物学正在对更多领域产生积极的影响,我相信这些技术未来将扮演更加重要的角色,也期待能够为推动学术界、产业界发展做出更大的贡献。”
《人民日报》曾评价:“在合成生物学和‘下一代工业生物技术’制造PHA生物塑料的道路上,陈国强团队使我国处于世界领先的水平。”目前,陈国强教授开发的技术已经在合成生物学产业中得以应用,国内已有多家企业如微构工场、微琪生物、安琪酵母等已应用最新的NGIB技术,进行规模化生物制造。可以说,受到国际认可,并实现了产业化落地的NGIB体系,前景无限可期。
原文转载自中国科技新闻网:https://www.zghy.org.cn/item/689912575852269568
3月24日,国际代谢工程学会(IMES)在其官方平台(https://www.aiche.org/community/bio/george-guo-qiang-chen)重磅宣布,将2023年度国际代谢工程奖(IMES Award)授予中国学者,清华大学生命科学学院教授、合成与系统生物学中心主任陈国强,以表彰他通过开发利用嗜盐菌和“下一代工业生物技术(NGIB)”对全球代谢工程领域所做出的卓越贡献。
国际代谢工程奖由代谢工程领域的国际权威学术组织国际代谢工程学会(IMES, International Metabolic Engineering Society)发起,每两年授予一位在代谢工程领域做出卓越贡献的研究人员,并在其和美国化学工程师协会(AIChE)共同举办的国际代谢工程大会(Metabolic Engineering Conference)上颁奖。

国际代谢工程学会(IMES)致力于促进和推进代谢工程,将其作为材料、药品、食品配料、化学品和燃料生物生产的一门辅助科学。2023年的第15届国际代谢工程大会将于6月11日至15日在新加坡举行,届时陈国强教授也将出席大会,并向全球学者介绍下一代工业生物技术(NGIB)在生物制造领域的最新进展。
IMES在官方网站上的展示
陈国强教授成为首位获得IMES Award的中国科学家
自2000年国际代谢工程奖正式颁发至今,陈国强教授成为了首位获得该奖项的中国科学家。此前获得该奖项的科学家包括生物化学工程先驱James E.Bailey、合成生物学领域权威Jay Keasling,以及多位美国工程院院士。
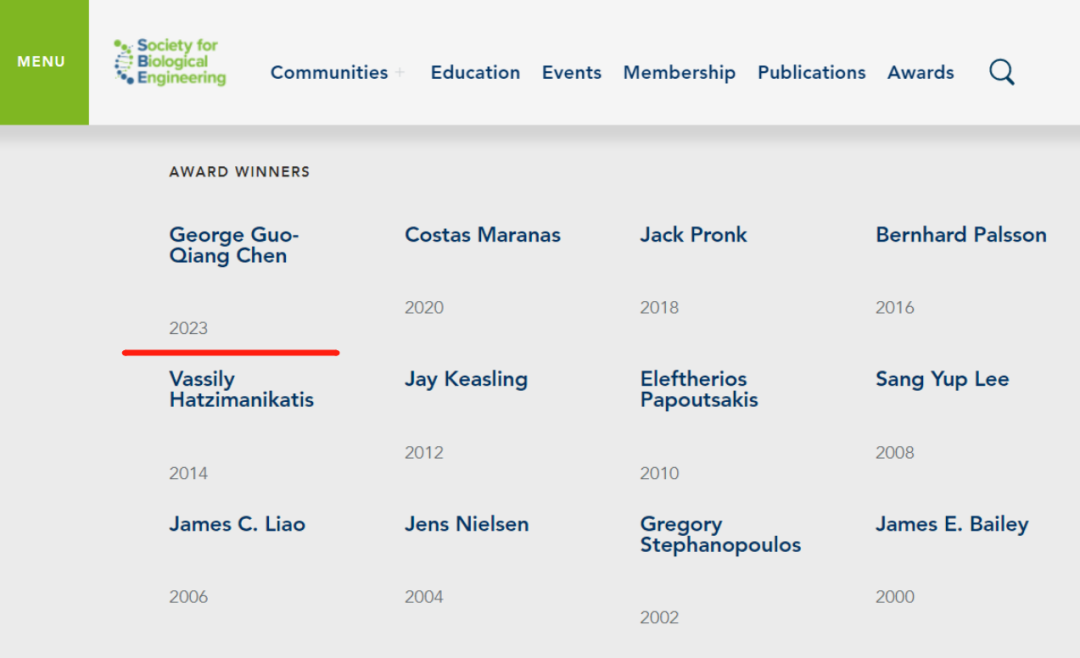
历届IMES Award获奖者名单
国际代谢工程奖评选委员会主席Sang Yup Lee教授表示:“陈国强教授一直致力用合成生物学的方式对嗜盐菌进行研究开发,以进行生产多种PHA和其他小分子化合物,对代谢工程领域做出了突出的贡献。目前,工程极端微生物和‘下一代工业生物技术’的概念已被广泛采用并应用于化合物的开放生产,陈国强教授获得国际代谢工程奖实至名归。”
NGIB将为生物制造领域带来颠覆性变革
2005年,陈国强教授和科研团队在位于世界上最酷热、最干燥的地区之一的新疆艾丁湖筛选出适应力最强的工业微生物菌株——嗜盐菌Halomonas,利用合成生物学和代谢工程学方法,通过DBTL(设计-构建-测试-学习)体系重新编辑嗜盐菌的基因,改造出适应能力更强、生长速度更快的菌株,成功开发了NGIB,覆盖了理论、模型、分子操作、实验室培养技术、中试技术及工业生产技术,以及部分产品的应用等。
相比于利用传统微生物底盘的工业生物技术(CIB),基于嗜盐菌的NGIB无需灭菌,生产过程可以开放和连续化,降低了能源和淡水消耗,并且降低了生物制造的复杂性和设备的制造成本,使生物制造产品竞争性得到增强。陈国强教授团队预测,NGIB能够将传统生物制造的能耗降低50%以上,并大幅提高生产效率。

合成生物学企业微构工场、微琪生物、安琪酵母、
麦得发、中粮生化等已应用最新的NGIB技术,
进行规模化生物制造
陈国强教授前期利用传统的微生物底盘对PHA材料进行过大规模的生产,发现了染菌问题很难解决,进而对嗜盐菌进行多年的代谢工程以及合成生物学改造,以令其更适用于大规模生物制造,包括重构Halomonas底盘细胞底物代谢途径,使其能利用多种底物,启动子工程和血红蛋白的配置以及新型反转搅拌发酵罐,使利用氧气效率大幅提升;重编群体效应代谢通路、形态学工程,改变细菌的生长方式、改造嗜盐菌的表面电荷,使细菌自凝絮,有利于连续发酵和菌分离;开放式的发酵减少了工艺流程和设备的复杂性等,目前该菌株已连续超过20代迭代。
合成生物学改造的嗜盐菌体系,也成功实现了各种生物及化学品的成功生产,括PHB、P34HB、P34HBHV、PHBHHX、PHB5HV、P3HP3HB等多种PHA材料。此外,还可用于生产戊二胺、四氢密呢、肌醇、氨基酸、3-轻基丙酸等产品。目前已获得的各种PHA材料正在开发用于医疗组织工程、功能材料、薄膜、纤维以及3D打印等领域,PHA材料的降解产物3-羟基丁酸及其衍生物也可用于研究治疗骨质疏松和老年痴呆等。

利用NGIB技术生产的PHA颗粒
不仅如此,在非粮碳源的利用上,陈国强教授团队也屡屡斩获突破。经过改造后的嗜盐细菌,可以利用秸秆糖、餐厨废料、废糖蜜、废工业乙酸等原料来合成PHA材料,为农业废弃秸秆的高值利用储备了先进技术,实现了非粮碳源生产。
目前,陈国强教授团队开发的技术已经在合成生物学产业中得到了应用,《人民日报》曾评价:“在合成生物学和‘下一代工业生物技术’制造PHA生物塑料的道路上,陈国强团队使我国处于世界领先的水平。”
个人简介
陈国强,1985年本科毕业于华南理工大学,1989年获得奥地利格拉茨(Graz)工业大学博士学位,1990至1994年在英国诺丁汉(Nottingham)大学和加拿大阿尔伯达(Alberta)大学做博士后研究,1994年回国入职清华大学生物系,现为清华大学生命科学学院教授、清华大学合成与系统生物学中心主任。

陈国强教授长期从事“生物合成PHA材料及其下一代工业生物技术”的研究,他在包括Chemical Reviews、Chemical Society Reviews、Science、Nature Communications等在内的多个国际学术期刊上发表微生物技术和生物材料相关论文380多篇,Web of Sciences记录论文被引用25000多次,已经获得50多项授权专利,以及50个公开专利。
陈国强教授以往获得的荣誉还包括:全国先进科技工作者(2016)、候德傍化工创新奖(2015)、首届闵恩泽能源化工杰出贡献奖(2013)、谈家祯生命科学创新奖(2011)、第八届中国青年科技奖(2003)、纽伦堡国际发明奖(2003)、茅以升科技奖(2003)、国家发明二等奖(排名第一)(2002)等。他还曾连续6年获得清华大学学生“良师益友”的光荣称号,进入清华大学“良师益友”名人堂,连续9年获得清华大学高论文他引的“梅贻琦奖”,连续7年获得Elsevier出版社生化与分子生物学高引用作者。此外,他还担任了Synthetic and Systems Biotechnology(SSB)的共同主编及多家国际、国内学术期刊的副主编职务。
原文转自:清华生命学院
清华大学生命科学学院教授陈国强受邀清华大学智能产业研究院(AIR),作题为《嗜盐菌合成生物学和“下一代工业生物技术”》的报告。

【讲者介绍】
陈国强教授是清华大学生命科学学院长聘教授,博士生导师,教育部长江学者特聘教授,清华合成与系统生物学中心主任;曾担任973计划、国家重点研发计划“合成生物学”专项首席科学家;长期从事“生物合成PHA材料及其下一代工业生物技术”的研究。
陈国强教授在国际学术期刊如Chemical Reviews, Chemical Society Reviews, Science, Advanced Materials, Advanced Science, Nucleic Acids Research, Nature Communications, Trends in Biotechnology, Biometaerials, Metabolic Engineering, Current Opinions in Biotechnology等上共发表微生物技术和生物材料相关论文350多篇,Web of Science纪录论文被引用两万两千多次(H指数为72)[Google Scholar引用六万多次,H指数100]。获得授权专利50多项,50个公开专利。他开发的技术已经在数家公司用于大规模生产微生物塑料聚羟基脂肪酸酯PHA。
【预约参会】
陈国强教授于3月20号(周一)下午14:00的讲座,欢迎大家预约线下参会,与讲师现场互动:
扫码线下预约参会

原文从“清华大学智能产业研究院”公众号转载,感兴趣的老师可以搜索并关注。
王海峰
清华大学 生命科学学院
博士,助理教授
教育经历
2000-2004 中国农业大学 本科
2004-2007 清华大学 硕士
2007-2013 加州大学戴维斯分校 博士
2013-2014 加州大学戴维斯分校 博士后
2014-2021 斯坦福大学 博士后
2021-现在 清华大学生命科学学院 助理教授
2021-现在 清华大学生命科学联合中心 研究员
研究方向:
本实验室将在哺乳动物细胞及模式生物中,开发利用CRISPR技术研究细胞发育生物学和疾病相关机理,并应用于精准医学诊断治疗。具体研究方向包括:
(1)开发CRISPR合成生物学工具从多维度研究基因组和转录组的调控机理;
(2)利用新型工具探求疾病发育过程中基因组和转录组的时空变化和基因调控的机理;
(3)精准医学:针对疾病相关的基因组或转录组异常,开发相应的诊断和靶向治疗方法。
代表性论文:
1,Wang H, Han M, Qi LS, Engineering 3D genome organization, Nature Review Genetics, 2021 Feb; PMID: 33558716;
2,Wang H, Nakamura M, Abbott TR, Zhao D, Luo K, Yu C, Nguyen CM, Lo A, Daley PT, La Russa M, Liu Y, Qi LS, CRISPR-mediated live imaging of genome editing and transcription. Science, 2019 Sep; Vol. 365, Issue 6459, pp. 1301-1305.
3,Wang H, Xu X, Nguyen CM, Liu Y, Gao Y, Lin X, Daley PT, Kipniss NH, La Russa M, Qi LS, CRISPR-Mediated Programmable 3D Genome Positioning and Nuclear Organization. Cell, 2018 Oct; 175, 1405-1417 e1414.
4,Wang H, La Russa M, Qi LS, CRISPR-Cas9 in genome editing and beyond. The Annual Review of Biochemistry, 2016 Aug; Vol. 85: 227-264.
5,Wang H, Brust-Mascher I and Scholey JM, The microtubule cross-linker Feo controls the midzone stability, motor composition, and elongation of the anaphase B spindle in Drosophila embryos. Molecular Biology of the Cell. 2015 Apr 15; 26(8):1452-62. PMID: 25694445. Selected as the Cover paper.
6,Wang H, Brust-Mascher I and Scholey JM, Sliding filaments and mitotic spindle organization, Nature Cell Biology, 2014 Aug; 16(8):737-739. PMID: 25082196.
7,Wang H, Brust-Mascher I, Civelekoglu-Scholey G and Scholey JM, Patronin mediates a switch from kinesin-13-dependent poleward flux to anaphase B spindle elongation, Journal of Cell Biology, 2013 Oct; 203(1):35-46. PMCID: PMC3798244.
联系方式:
邮箱:该Email地址已收到反垃圾邮件插件保护。要显示它您需要在浏览器中启用JavaScript。
2021年5月11日,聚焦合成生物学领域的Synbio Hive 创新孵化平台首场路演在清华大学生命学院顺利举行。该平台的主题是“Engineering Biology, Engineering Tomorrow”,致力于打造成为中国本土的合成生物领域顶级平台。路演吸引了中心多位老师和同学、产业和资本界代表等多位业内人士关注并到场交流。
据介绍,Synbio Hive平台旗下包括创新大赛、创业大赛、企业孵化、学术峰会、产业峰会等不同板块。平台将以大赛作为依托,希望打通中国合成生物领域的产、学、研、创、投通道,真正形成中国合成生物的创新落地生态闭环,让合成生物领域的创新想法有落地的支撑和可能,以产业需求驱动源头创新。
本场路演由合成与系统生物学中心主任陈国强教授主持并致开幕词。陈国强教授开场先简要介绍了Synbio Hive成立的初衷,并希望不断集思广益改善平台赛事的举办形式和发展;随后生命学院副院长刘栋教授从广为熟知的iGEM赛事出发,结合中国特色,提出打造中国独有的合成生物学赛事平台的重要性,并当场表示会对Synbio Hive的发展提供强力的支持和帮助。
在介绍了Synbio Hive的具体运营模式之后,包括于慧敏教授、李春教授、张翀副教授以及张数一副教授在内的多位中心老师对该赛事平台进行了点评,并提出较多宝贵而又富有建设性的意见和建议,并希望能不断推动该平台的又好又快发展。以中石化资本、诺维信为代表的资本和产业界同仁也提出了较为针对性的研究成果到产业落地的意见,从而不断改善Synbio Hive平台的建设和发展。

The provision of new antibiotics to combat antimicrobial resistance (AMR) and to treat neglected tropical diseases (NTD), which are problematic in the developing world, is a major global challenge. Most of the of antibiotics in clinical use today are derived from microbial secondary metabolites (natural products). In addition to essential antibacterial, antifungal and antiparasitic agents, microbial natural products have been developed as antitumour, antiviral, immunosuppressive agents and as cholesterol lowering agents. In many cases the natural products are produced in very small quantities by microbial species that are difficult to cultivate or genetically manipulate. In addition to this, genome sequencing reveals many bacterial strains possess cryptic biosynthetic gene clusters (BGC) that appear to be silent when cultivated in the laboratory. These strains possess the machinery to produce bioactive natural products, but the biosynthetic genes are not expressed in the native hosts. One way to increase production levels, and also to activate expression of cryptic/unproductive BGC, is to transfer the BGC into heterologous host strains which are more genetically tractable and easier to cultivate. Unfortunately, there are a limited number of well characterised hosts available and some of these are not necessarily ideal for production of certain natural product scaffolds. For example, Escherichia coli and yeast have been widely used, but these strains are not known to produce large numbers of secondary metabolites and production of certain types of natural products can be problematic, particularly those generated by nonribosomal peptide synthetase (NRPS), polyketide synthase (PKS) and hybrid NRPS-PKS assembly lines. In this project we will exploit recent advances in synthetic biology to develop new genetic tools for heterologous expression and manipulation of microbial BGC in new Halomonas host strains to produce antibiotics and other important bioactive natural products. Halomonas are halophiles (tolerate high salinity) and can be easily cultivated under nonsterile conditions. In light of this, Halomonas sp. have emerged as a useful host for production of low molecular weight metabolites and also biopolymers. In this project we aim to develop Halomonas further as heterologous host for production of microbial NRPS, PKS and hybrid NRPS-PKS secondary metabolites, which provide many valuable antibiotics and other important therapeutic agents.
The project will involve a collaboration between the Micklefield lab at the Manchester Institute of Biotechnology (MIB) and George Chen, Director of the Center for Synthetic and Systems Biology (CSSB) at Tsinghua University in Beijing. The student will spend two years in Manchester and two years in Beijing. Training in Manchester will cover natural products chemistry, protein engineering, directed evolution, enzyme characterisation and enzyme assays. In Singapore the student will develop further skills in synthetic biology, molecular biology and microbiology, including manipulation of Halomonas bacteria. Candidates are not expected to have expertise in these areas at the outset; above all, scientific curiosity and a desire to work in a multidisciplinary environment are most important. Candidates with a degree in Chemistry, Biochemistry or Biological Sciences and an interest in enzyme catalysis, biosynthesis (natural products), microbiology, synthetic biology or a related science are encouraged to apply.
Entry Requirements
Students must meet the entry requirements of both universities, and will be registered at both institutions in the first year of study.
Applicants should hold (or be about to obtain) a minimum 2:1 bachelor's degree (or overseas equivalent), in a relevant discipline, plus a master's degree or extensive research experience. Applicants can be internal or external to The University of Manchester. For applicants whose first language is not English, we require a minimum IELTS score of 6.5.
For more information see:
http://www.manchester.ac.uk/research/Jason.micklefield/
http://www.micklefieldlab.chemistry.manchester.ac.uk
http://life.tsinghua.edu.cn/lifeen/info/1034/1088.htm
synbiodual
The provision of new antibiotics to combat antimicrobial resistance (AMR) and to treat neglected tropical diseases (NTD), which are problematic in the developing world, is a major global challenge. Most of the of antibiotics in clinical use today are derived from microbial secondary metabolites (natural products). In addition to essential antibacterial, antifungal and antiparasitic agents, microbial natural products have been developed as antitumour, antiviral, immunosuppressive agents and as cholesterol lowering agents. In many cases the natural products are produced in very small quantities by microbial species that are difficult to cultivate or genetically manipulate. In addition to this, genome sequencing reveals many bacterial strains possess cryptic biosynthetic gene clusters (BGC) that appear to be silent when cultivated in the laboratory. These strains possess the machinery to produce bioactive natural products, but the biosynthetic genes are not expressed in the native hosts. One way to increase production levels, and also to activate expression of cryptic/unproductive BGC, is to transfer the BGC into heterologous host strains which are more genetically tractable and easier to cultivate. Unfortunately, there are a limited number of well characterised hosts available and some of these are not necessarily ideal for production of certain natural product scaffolds. For example, Escherichia coli and yeast have been widely used, but these strains are not known to produce large numbers of secondary metabolites and production of certain types of natural products can be problematic, particularly those generated by nonribosomal peptide synthetase (NRPS), polyketide synthase (PKS) and hybrid NRPS-PKS assembly lines. In this project we will exploit recent advances in synthetic biology to develop new genetic tools for heterologous expression and manipulation of microbial BGC in new Halomonas host strains to produce antibiotics and other important bioactive natural products. Halomonas are halophiles (tolerate high salinity) and can be easily cultivated under nonsterile conditions. In light of this, Halomonas sp. have emerged as a useful host for production of low molecular weight metabolites and also biopolymers. In this project we aim to develop Halomonas further as heterologous host for production of microbial NRPS, PKS and hybrid NRPS-PKS secondary metabolites, which provide many valuable antibiotics and other important therapeutic agents.
The project will involve a collaboration between the Micklefield lab at the Manchester Institute of Biotechnology (MIB) and George Chen, Director of the Center for Synthetic and Systems Biology (CSSB) at Tsinghua University in Beijing. The student will spend two years in Manchester and two years in Beijing. Training in Manchester will cover natural products chemistry, protein engineering, directed evolution, enzyme characterisation and enzyme assays. In Singapore the student will develop further skills in synthetic biology, molecular biology and microbiology, including manipulation of Halomonas bacteria. Candidates are not expected to have expertise in these areas at the outset; above all, scientific curiosity and a desire to work in a multidisciplinary environment are most important. Candidates with a degree in Chemistry, Biochemistry or Biological Sciences and an interest in enzyme catalysis, biosynthesis (natural products), microbiology, synthetic biology or a related science are encouraged to apply.
Entry Requirements
Students must meet the entry requirements of both universities, and will be registered at both institutions in the first year of study.
Applicants should hold (or be about to obtain) a minimum 2:1 bachelor's degree (or overseas equivalent), in a relevant discipline, plus a master's degree or extensive research experience. Applicants can be internal or external to The University of Manchester. For applicants whose first language is not English, we require a minimum IELTS score of 6.5.
For more information see:
http://www.manchester.ac.uk/research/Jason.micklefield/
http://www.micklefieldlab.chemistry.manchester.ac.uk
http://life.tsinghua.edu.cn/lifeen/info/1034/1088.htm
synbiodual
佛山市第一人民医院始建于1881年,跨越三个世纪,是一所集医、教、研为一体的大型现代化三级甲等综合医院。临床上在微创、介入、器官移植等多领域技术居省内乃至国内先进水平。曾在国内率先开展内镜(腹腔镜)手术,并成为卫生部妇科内镜培训基地。医院先后荣获“全国办得最好的十二家专区医院之一”、“全国卫生系统先进集体”、“全国医院文化先进单位”、“全国医院文化建设先进集体”、“全国教科文卫体系统先进工会组织”、“全国厂务公开先进基层单位”、“全国改革创新医院”、“全国首批无烟医院”等荣誉称号。
为满足医院科研的发展和需要,现特和清华大学张奇伟实验室及高军涛副研究员合作,招聘医学、细胞生物学、生物技术、免疫学等相关专业研究助理2名。
工作地点:广东,佛山,佛山市第一人民医院
开始时间:2021年1月1号,也可随时上岗
工作地点:佛山,佛山市第一人民医院
招聘人数:2 人
岗位职责:
若不具备相关实验技术,可以进行岗前技术培训。
上岗时间:2021年1月1号,或随时上岗。
申请资格:
相关待遇和福利:
享受佛山市第一人民医院和清华大学项目聘用合同制人员相关待遇(包括四险一金、基本工资、带薪年假、季度奖金、年终奖金等)、享受佛山市第一人民医院科研资源,以有助于未来提升自己(读研或进修等)。
申请材料:
1. 个人简历,请重点突出相关科研经历和已熟练掌握的生物实验技能。
2. 个人联系方式,包括Email、电话。
请将申请材料发至:罗老师,该Email地址已收到反垃圾邮件插件保护。要显示它您需要在浏览器中启用JavaScript。
工作地点:北京,清华大学;招聘人数: 1 人
上岗时间:2021年1月1号,或者随时。
岗位职责:
申请资格:
1、品德端正,道德感强。爱岗敬业,团结他人。
2、备选专业一:具有光电专业、生物医学工程、生物影像相关专业的本科或硕士学位,具有丰富的光电知识和实验技能,熟练搭建新光路、操作各种显微镜(包括共聚焦、超分辨和电镜的操作和样品制备)、具有丰富实验经验的博士毕业生将优先考虑。
3、备选专业二:具有分子生物学、细胞生物学、生物技术等专业的本科或硕士学位,具有基因表达调控、单细胞、多组学、肿瘤等一个或多个领域的丰富经验,可以熟练进行三维基因组等多组学分子生物学和细胞生物学的实验操作(文库构建、高通量测序、样品制备等)。
3、能稳定工作两年及以上。
4、有良好的英文文献阅读能力和交流能力。
5、动手能力强,拥有熟练的实验技能。
6、获过更多奖励、有特殊技能的,将酌情考虑。
相关待遇和福利:
享受清华大学项目聘用合同制人员相关待遇(包括四险一金、基本工资、带薪年假、季度奖金、年终奖金等)、享受清华大学校内相关教育和科研资源,以有助于未来提升自己(读博或者更好的发展)。
申请材料:
1. 个人简历,请重点突出生物学研究相关的研究经历和已熟练掌握的生物实验技能。
2. 成绩单扫描件、论文摘要。
3. 个人联系方式,包括Email、电话。
请将申请材料发至: 该Email地址已收到反垃圾邮件插件保护。要显示它您需要在浏览器中启用JavaScript。
清华大学合成与系统生物学中心高军涛副研究员
招聘研究助理
(生物技术/分子生物学方向)
工作地点:北京,清华大学;招聘人数: 1 人
岗位职责:
上岗时间:2021年1月1号,或随时上岗。
申请资格:
相关待遇和福利:
享受清华大学项目聘用合同制人员相关待遇(包括四险一金、基本工资、带薪年假、季度奖金、年终奖金等)、享受清华大学校内相关教育和科研资源,以有助于未来提升自己(读博或者更好的发展)。
申请材料:
1. 个人简历,请重点突出生物学研究相关的研究经历和已熟练掌握的生物实验技能。
2. 成绩单扫描件、论文摘要。
3. 个人联系方式,包括Email、电话。
请将申请材料发至: 该Email地址已收到反垃圾邮件插件保护。要显示它您需要在浏览器中启用JavaScript。