

近日,清华大学自动化系、北京信息科学与技术国家研究中心谢震课题组在一项最新研究中,开发了一种核糖体内部进入位点(internal ribosome entry site, IRES)的工程改造技术(programmable miRNA-responsive IRES translation activation and repression, PROMITAR),实现了仅用单个环状 RNA 分子即可感应多种细胞内源微小 RNA(miRNA)信号,控制 IRES 元件在特定细胞中的翻译活性。相关研究成果以“在哺乳动物细胞中理性设计响应 microRNA 的可编程翻译调控开关”(Rational design of microRNA-responsive switch for programmable translational control in mammalian cells)为题,于 11 月 8 日发表于《自然·通讯》(Nature Communications)期刊。
与线性 mRNA 相比,环状 RNA(circRNA)更稳定,在哺乳动物细胞内的持续时间更长。因此 circRNA 被认为是一种很有前景的线性 mRNA 的替代物。迄今为止,合成生物学家已经开发出了多种在线性 mRNA 和 circRNA 中调控基因表达的策略。但这些方法通常需要引入额外的 RNA 结合蛋白(RBP)的适配体(aptamer)或 miRNA 结合位点进行翻译抑制(OFF-switch),并需要串联多个翻译抑制来实现翻译激活(ON-switch),增加了 RNA 基因线路的复杂性。而前人报道的由 miRNA 激活 RNA 翻译的策略依赖于 miRNA 切割来释放聚腺苷尾部(polyA 尾)或切除线性 mRNA 的降解域,降低了 circRNA 在细胞中的稳定性。
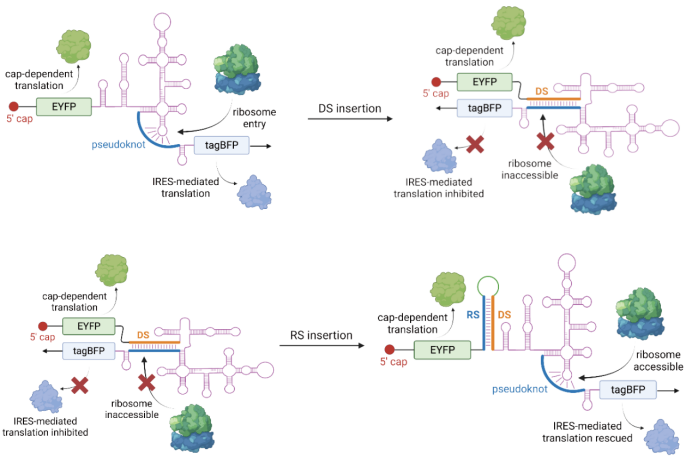
▲图 1|通过设计 DS 和 RS 序列实现 HCV-IRES 结构和翻译功能的破坏与恢复
在本研究中,研究人员设计了控制 RNA 翻译活性的 PROMITAR 技术平台。该平台包含三部分:感应 miRNA 的 IRES 翻译激活模块(MITA)、感应 miRNA 的 IRES 翻译抑制模块(MITR)和目标基因编码序列。在该设计策略中,不同 miRNA 的存在或缺失会触发 MITA 或 MITR 的激活,从而实现目标基因的翻译激活或翻译抑制。基于这一设计理念,研究人员以丙肝病毒(HCV)的 IRES 序列为基础,通过在 IRES 上游插入一段与 IRES 内部关键的假结(pseudoknot)部位互补配对的序列(称为“破坏序列”,DS),来打开 IRES 二级结构,从而抑制 IRES 介导的基因翻译。然后,在该“破坏序列”(DS)上游插入一段与之互补的“修复序列”(RS),利用 RS-DS 互补配对释放假结序列,恢复 IRES 的结构并重新激活翻译。在“修复序列”附近设计特殊的 RNA 二级结构,并在该二级结构中融入特定的 miRNA 识别序列,利用 miRNA“海绵”(miRNA sponge)机制即可实现 miRNA 响应的 IRES 翻译激活单元。进一步通过在 IRES 两侧插入 miRNA 的完全互补配对序列,利用 RNAi 机制即可同时实现 miRNA 响应的 IRES 翻译抑制。

▲图 2|设计包含特定 miRNA 结合位点的二级结构实现响应特定 miRNA 的 IRES 翻译激活
基于该平台,研究人员成功构建了具有逻辑运算门和细胞分类功能的 circRNA,并在哺乳动物细胞中进行了验证。结果表明,这些 circRNA 分子可以准确响应内源 miRNA 的变化,从而实现对特定细胞类型的成功识别。研究人员还将 Gasdermin D 蛋白的 N 端序列编码到 circRNA中,实现了在目标肝癌细胞中诱导细胞焦亡,实现肿瘤细胞的特异性杀伤。展示了该平台的潜在医学应用价值。另外,研究人员还验证了这一设计策略可以推广至其他病毒类型的 IRES 序列的工程改造,展示了该平台的通用性。该研究成果不仅拓展了 RNA 翻译控制的合成生物学工具箱,为程序化的细胞功能改造提供了一种创新方法,也为 RNA 药物开发提供了新的思路。
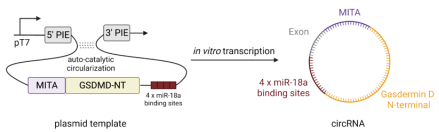
▲图 3|设计含有 miRNA 激活(MITA)和抑制(4 x miR-18a binding sites)元件的 circRNA
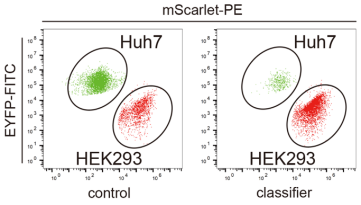
▲图 4|具有细胞类型分类功能的 circRNA 在肝癌细胞中诱导细胞焦亡
清华大学自动化系谢震副教授为论文的通讯作者,清华大学自动化系博士研究生宁辉、北京合生基因科技有限公司刘淦博士为论文的共同第一作者,清华大学自动化系李磊博士、北京合生基因科技有限公司刘强、黄慧雅博士参与了该项目研究。该研究得到国家重点研发计划、国家自然科学基金、北京清华工业开发研究院、清华大学春风基金和北京信息科学技术国家研究中心的资助。
参考资料:1.https://www.nature.com/articles/s41467-023-43065-w
免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。